+ H& W2 I; X6 F5 j$ m, Q6 s
% R- M; J3 t: [9 K/ p+ `
华盛顿特区(2016年4月21日)——两项由美国ALS协会资助的独立研究(一项由佛罗里达大学Laura Ranum博士领导,另一项由加州大学圣迭戈分校Don Cleveland博士和麻省总医院Clotilde Lagier-Tourenne博士领导)开发出新的C9orf72突变小鼠模型,表现出肌萎缩侧索硬化(ALS)和额颞叶痴呆(FTD)中的神经变性退化和运动及认知缺陷。此外,其中一组表明,小鼠中的这些问题可以通过对抗突变基因的反义疗法进行改善。
( \& K7 f' R& J) e4 |; @4 k
“这些研究代表着理解C9orf72基因突变后果和开发疗法工作中的重大进展” ALS协会首席科学家Lucie Bruijn博士说道。
2 k( b% W. p# r0 V) w: d5 Q
ALS(肌萎缩侧索硬化),也就是卢伽雷氏症,是一种侵犯大脑和脊髓中神经元(神经细胞)的进行性神经退行性疾病。最终,ALS患者会失去发起和控制肌肉活动的能力,导致完全瘫痪和死亡。该病目前尚无治愈或有效治疗方法。 $ W0 v0 M( P) s9 m( X' J9 F2 w
C9orf72基因的正常功能目前未知,但该基因中的扩张突变是ALS和FTD最常见的遗传致病因。该基因扩张于2011年被发现,其他研究团队已经开发出该基因的小鼠模型,并着手探索突变的后果。新开发的模型将显著增加展示由C9orf72突变导致的ALS的能力。 , |% c0 t$ L6 S+ Z- F5 N7 K+ t" @0 M$ d
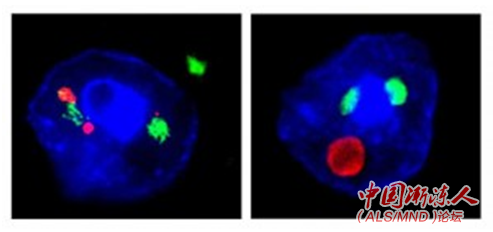
在第一项新研究中,Yuangjing Liu博士和首席研究员、佛罗里达大学Laura Ranum博士及同事们将携带全长C9orf72基因的大量DNA的载体“细菌人工染色体(bacterial artificial chromosome)”注入小鼠细胞。这些小鼠发展出突变细胞的特征,包括被称为“聚集点(foci)”的RNA积聚和非标准蛋白质(RNA蛋白)的表达,这两方面都被认为会促进疾病的发展。这些小鼠还表现出生存期减少、瘫痪麻痹、运动神经元丢失、焦虑(与FTD有关的认知特征)和多个大脑区域的神经变性退化。 3 x/ c x; T# C$ ^# C; `
在第二项研究中,共同作者Jie Jang博士、QiangZhu博士和Tania Gendron博士与主要研究员Don Cleveland博士和Clotilde Lagier-Tourenne博士以及同事们,创造出多个小鼠模型,其中一些减少表达或不表达正常C9orf72基因,而其他的则表达突变C9orf72基因。Jang、 Zhu和Cleveland博士来自加州大学圣迭戈分校,Gendron博士来自梅奥诊所,Lagier-Tourenne博士来自麻省总医院。Cleveland博士的实验室是神经协作(NeuroCollaborative)项目的一部分。
/ i" R1 E, o& u \- y% L5 w
3 u5 w g8 h8 Z6 N( L" m: u6 f
来自这些小鼠模型的发现表明,该基因表达的部分或完全丢失都不会导致神经变性退化。相反,正如Ranum博士研究所发现的,突变基因的表达会导致ALS-样和FTD-样特征,包括焦虑。重要的是,这些特征能够通过反义寡核苷酸(ASOs)治疗显著减少。ASOs治疗允许正常基因表达,但可以防止产生自突变基因的长RNA链的积聚。ASO技术致力于通过防止蛋白质被创建而消除蛋白质。
) b, B) Y, \3 Z
“这些模型为更充分地理解C9orf72基因突变的影响提供了重要的新方法,将直接促进对反义疗法的进一步开发,从而减少这些影响” Bruijn博士说,“有趣的是,这些模型和更早发表的C9orf72小鼠模型都略有不同。理解这些差异可能为疾病过程提供进一步的见解。”
2 s3 [- Z# l6 k0 O, S
' G' o) @% `( |( t! K6 M$ U6 L
关于美国ALS协会(The ALS Association)
* X W7 Q2 w+ _; E- ~2 G' b9 Q) D
ALS协会是美国唯一在各条战线上抗击ALS的国家性非营利组织。通过引领全球研究,利用全国性分会网络为ALS患者提供支持,利用认证的临床护理中心协调多学科综合护理,培育政府合作关系,ALS协会在为ALS患者构建希望、提高生活质量的同时,积极寻找新的治疗和治愈方法。更多信息可见协会网站:www.alsa.org
- f* Q2 j. O$ [- E2 u: j" A& E
7 u6 i' r( R; N: P | 




 发表于 2016-4-27 21:33:33
发表于 2016-4-27 21:33:33

 楼主
楼主


 两个大沙发!
两个大沙发!
 发表于 2016-4-28 07:43:03
发表于 2016-4-28 07:43:03

 发表于 2016-4-28 09:17:21
发表于 2016-4-28 09:17:21


