* L1 S$ d$ E f0 `9 F7 R( F( z- g4 M2 h( Q/ g3 v
在2016年4月21日发表于《神经元(Neuron)》期刊的研究中,佛罗里达大学健康(University of Florida Health,UF Health)研究人员开发出了一种独特的小鼠模型,将允许世界各地的研究人员更好地研究肌萎缩侧索硬化(ALS)和额颞叶痴呆(FTD)的基因起源和潜在疗法。
/ a# m7 ^8 @6 ^5 I ?) `
新的小鼠模型意义重大,因为它能够紧密地再现携带C9orf72基因突变的ALS患者的症状和基因表达模式。 7 o7 W* b$ n% [4 h
1 E6 a" i& Z! O5 p" F# h
UF神经遗传学中心主任、UF遗传学研究所教员、UF医学院分子遗传学和微生物学教授Laura P.W.Ranum博士表示:获得能够再现这两种疾病如何影响大脑和脊髓中神经细胞及通路的小鼠模型,对于理解患者中的疾病触发因素和疗法开发是至关重要的。
+ @; w+ v' D' n4 H/ H: m
该研究领导作者Yuanjing Liu博士最近毕业于UF生物医学科学跨学科项目,与研究生Amrutha Pattamatta及UF的其他研究人员密切合作,生成并塑造了小鼠模型的特性。该团队花费近4年时间开发这种携带C9orf72基因扩张突变的小鼠模型。根据ALS协会的统计数据,这种突变是ALS最常见的遗传致病因,涉及40%的家族型病例。该突变也是遗传性痴呆的常见致病因。
. j/ d6 [- _9 R1 E, m/ o* d. u
+ Y( i5 M+ C3 ]* h9 x' i. d
Laura P.W. Ranum博士、Yuanjing Liu博士和研究生Amrutha Pattamatta
1 f, F- H5 s" L6 D
ALS会杀死从大脑伸展到脊髓和从脊髓到肌肉的神经细胞,导致患者肌肉萎缩、瘫痪和死亡。据估计,在任何时点,美国都有3万人罹患该病,预期寿命通常为2到5年。 5 W% e0 M% w. v- C# `$ I. I) k
虽然其他科学家已经开发了关注于不同ALS-相关基因的小鼠模型,但UF Health研究人员首次培养出关注于C9orf72基因的小鼠模型,紧密模拟ALS和FTD的特征,包括麻痹和痴呆。新的小鼠模型将允许研究人员理解相同的基因突变如何导致一些患者出现瘫痪问题,另一些人出现认知和行为问题,还有的人则不受疾病影响。这些小鼠表现出有问题RNA的积聚和蛋白质团块的形成,涉嫌促进疾病的发展。
- Z0 n6 D$ E) ?5 R, N( o1 Y
由于ALS和FTD属于遗传上复杂的疾病,难以在人类中进行研究,因此小鼠模型将使研究人员能够精确梳理该基因突变如何导致疾病。C9orf72基因至少产生8种不同的突变体产物,新的小鼠模型将帮助研究人员理解哪些产物对于导致疾病是最重要的。还能够帮助研究人员理解更多关于一个大脑特定区域所发生的问题,在该区域中,健康细胞存在于已经死亡的细胞旁边。 3 l! \* B& B, K4 H3 Z1 E. X$ |. L
' K# C; K3 d$ p+ R& f
“我感到非常兴奋,因为该突变产生的两种突变体RNAs中的一种会在易受疾病影响和死亡的神经元中积累。这为我们未来旨在为患者开发疗法的研究提供了重要的线索” Liu说道。
- z4 s9 V( ~6 B8 C
同样地,Ranum被另一种现象所吸引:20%携带该突变基因的小鼠没有发展出ALS或FTD。这种现象与人类中的状况相似,人类中也存在携带C9orf72突变而不发展出疾病的人群子集。这表明某些保护性元素在发挥作用,如果能够理解这些元素,就可能预防疾病的发生,她说道。 - z7 b g- I4 p& _) V0 C
Ranum表示,她的团队已经使新的小鼠模型得到应用,包括与私营企业合作进行旨在逆转或防止疾病的研究。
# C8 j" W7 m+ ]3 g7 B% \7 {
- z+ A C0 }& Q8 k' Y; p
8 z, R% a1 j' |+ h) l | 




 发表于 2016-4-22 18:49:06
发表于 2016-4-22 18:49:06


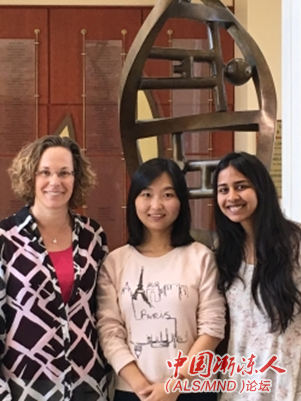


 发表于 2016-4-22 20:12:30
发表于 2016-4-22 20:12:30



 发表于 2016-4-23 04:48:59
发表于 2016-4-23 04:48:59


 楼主
楼主

 小老鼠!你咋不属大象!
小老鼠!你咋不属大象!