' T, _" t4 v# l6 _5 d6 J) ]) W; H. `7 Q
3 d( T9 q, Y9 k$ _; R. `* a
一项最近发表于《细胞•报告》(Cell Reports)杂志的研究报告,新识别的GLT8D1酶编码序列中的新基因突变与遗传性肌萎缩侧索硬化(ALS)有关。
: ^) F7 j+ J0 C( p7 Y5 ?
0 b* J% P, S8 q4 T7 ^& {0 {
英国谢菲尔德大学的研究人员和他们的合作者们发现,这些GLT8D1基因变异会妨碍GLT8D1酶的正常功能,与实验斑马鱼模型中的细胞毒性和ALS样运动缺陷增加相关联。
% \0 @) I0 b" K3 X8 O# y
研究人员对一个家族中两名被诊断出患有ALS的相关个体进行了基因筛查。分析揭示出影响不同基因的5种可能导致ALS的基因变异。
7 Q4 B9 d# }/ U' G. t# R
第三名家族成员也开始出现单侧无力和上运动神经细胞功能障碍的体征,提示ALS,但尚未确诊。对该家族成员的基因分析也显示出之前在GLT8D1和ARPP21基因中识别的相同突变。
' Y& n$ K8 S+ j v# t
为了进一步探索这些新识别突变在导致ALS方面的潜在作用,研究团队对英格兰北部103例家族性和年轻散发性ALS病例的样本进行了重复筛查。
4 M# {% b7 n- ?9 I0 c
他们发现了另外5个病例,其中4例携带与之前家族中识别的相同的GLT8D1基因突变,还有一例携带相同基因中新的有害突变。
1 R5 Q6 L8 {% t% r) A# x
9 ^8 U" V) \9 u7 ~6 q8 L
研究人员发现,GLT8D1突变的存在与ALS发病风险增加20.3倍有关。当与ARPP21基因突变合并存在,GLT8D1突变会导致ALS风险增加54.1倍
8 d4 e+ W- u7 u/ D
“在我们对MND进行细分并寻找新治疗策略的过程中,患者的基因筛查正变得越来越重要,” 该研究高级作者、谢菲尔德大学转化神经科学研究所(SITraN)兼NIHR谢菲尔德生物医学研究中心主任Pamela Shaw博士说道。
+ O5 a! _! g+ a9 r9 W- D# _' w
“基础科学突破,例如这种对MND新致病基因的发现,对于帮助我们理解疾病机制至关重要,为找到潜在新疗法铺平了道路,” Shaw博士说道。
* q7 F$ g3 h/ n, _
对这些携带GLT8D1突变的ALS患者的临床表现评估表明,总体而言,他们的疾病表现在ALS的预期谱系范围内。不过,同时携带GLT8D1和ARPP21突变的患者比只有一个基因受影响的患者病情更严重。
" @( o4 D. C: s6 ]8 a% F4 ~+ C
为了更好地理解GLT8D1突变的影响,研究团队使用ALS细胞和斑马鱼模型进行了几次实验。
/ X! [6 c& N/ H, b
( J- s6 }9 D4 q
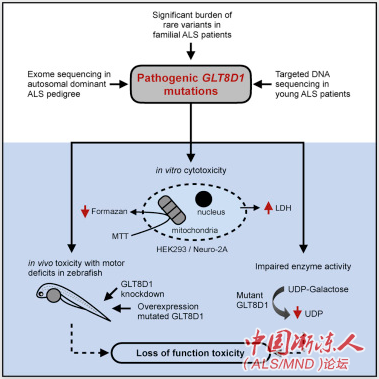
他们的实验表明,新发现的GLT8D1突变对细胞代谢和生存具有显著的负面影响。此外,GLT8D1基因突变的存在或基因抑制GLT8D1酶的产生,会严重影响斑马鱼胚胎的活动性。
$ r6 r( Q% h% |
目前还不清楚GLT8D1酶的作用,尽管它存在于人体几个组织中。通过进一步的分析,研究团队发现GLT8D1基因突变会妨碍GLT8D1酶的正常活性,这可能与检测到的ALS相关毒性和运动细胞损伤直接相关。
7 c1 O+ `& R; J+ E
“我们的功能数据确认了所发现的GLT8D1基因突变在体内和体外的分子毒性,” 研究人员写道。
v$ B6 b) F" ]6 {: Y
“我们的发现将GLT8D1糖基转移酶活性定位于ALS发病机制的上游,使其成为一个有吸引力的治疗靶点,” 他们补充道。
- M$ L8 d5 O. \6 t
& V D/ h# f5 a 




 发表于 2019-3-13 01:01:36
发表于 2019-3-13 01:01:36


 发表于 2019-3-13 01:27:42
发表于 2019-3-13 01:27:42

