|
NurOwn被证明是安全而耐受性良好的 与安慰剂比较,在所有时间点对NurOwn的更高应答证明了临床上有意义的益处 电话会议和现场网络直播在美国东部时间上午10点进行 9 e$ o% b' ~# X* ]/ ~
美国新泽西州哈肯萨克市&以色列佩塔提克瓦,2016年7月18日——BrainStorm细胞疗法公司(BrainStorm Cell Therapeutics Inc.)今日宣布了最近在美国完成的NurOwn治疗肌萎缩侧索硬化(ALS)患者的随机、双盲、安慰剂对照2期研究结果。研究实现其主要目的,证明NurOwn是安全而耐受性良好的。NurOwn也达到了多个次要有效性终点,所获得的明确证据表明了临床上有意义的益处。值得注意的是,在研究24周的所有时间点,与安慰剂相比,NurOwn治疗的患者拥有更高的应答率。
2 V7 l" x2 m2 I
“2期数据表明,NurOwn细胞疗法是安全的,在ALS功能评定量表-修订(ALSFRS-R)和脑脊液(CSF)生物标志物方面,单次治疗都能够产生短暂而临床上有意义的有益应答,这让我们感到非常鼓舞” 麻省大学医学中心神经内科主任、医学院教授、该试验研究者Robert H. Brown博士说,“这些激动人心的结果清楚地表明,该疗法适合于进行重复给药的更长期的研究。”
2 @0 g' h; ], n: x- N4 K
“试验结果让我们感到兴奋,提供了NurOwn安全性、初步有效性和生物效应方面的重要信息”哈佛医学院神经病学教授、麻省总医院神经内科主任Merit E. Cudkowicz博士说,“治疗组中更多的参试者病情发展减缓,而且没有安全性问题。两周后观察到的脑脊液中生长因子水平增加和炎症标志物减少,是鼓舞人心的生物效应证据。基于这些结果,在8到12周重复给药和更大的验证性试验是必要的。我期待继续与BrainStorm公司密切合作,为ALS患者开发NurOwn疗法。” : ~9 K* B5 |: S2 y( y
“在开展了近30年的ALS临床研究后,这些试验结果让我非常鼓舞和兴奋” 梅奥诊所再生医学中心发现主任、神经病学教授Anthony J. Windebank博士说,“明确的迹象显示出积极的有效性信号,我们在梅奥诊所渴望尽可能快地推进到下一阶段研究。” 7 G8 l5 ~5 t8 v- `) o4 s
“BrainStorm公司研究中患者对治疗的耐受性非常好,没有与治疗相关的严重不良事件。安全特性确实提供了继续研究这种方法作为ALS疗法的机会”该研究数据安全监督委员会(DSMB)主席、德克萨斯大学健康科学中心首席医疗官、神经病学和耳鼻喉科教授Carlayne E. Jackson博士说道。
. }% |3 K7 q [9 { P
“我要感谢参与这项临床试验的患者、研究者、DSMB成员和所有为成功完成试验做出贡献的人们。这些数据为我们深入了解NurOwn有益的治疗效果提供了宝贵的见解” BrainStorm公司首席执行官Chaim Lebovits说,“这项研究达到了目的,证明了NurOwn的安全性及其为ALS患者提供临床益处的能力,而且最重要的是,将帮助我们确定研究人群并设计NurOwn多次给药治疗ALS的关键研究”。
% S) _2 j9 i- ~, g0 b( T0 N. O$ E
研究设计 4 i) q% K4 F" n: k2 T) Y; o/ r
这项2期试验是一项随机、双盲、安慰剂对照的多中心研究,设计为针对48位ALS患者评估NurOwn的安全性和有效性。该试验在美国三个研究基地进行:麻省总医院、麻省大学医学院和梅奥诊所。患者被随机分配接受NurOwn细胞肌肉和鞘内联合注射(n=36)或安慰剂治疗(n=12)。在治疗前大约三个月进行每月随访,治疗后进行六个月的随访,分别在第2、4、8、12、16和24周进行评估。该研究的主要目的是(评估)安全性和耐受性。预先规定的有效性分析是:ALSFRS-R得分斜率的改变,缓慢肺活量(SVC)改变和肌肉力量,应答者分析(治疗后获得改善的参试者与治疗前参试者相比的百分比)和一个子组分析(排除病情发展缓慢、不太可能检测到NurOwn治疗益处的患者)。鉴于该研究的探索性质,统计显著性被定义为单边p值< 0.1使用费舍尔精确检验(Fisher'sexact test)。
+ X: |# U f! c1 {* E
ALSFRS-R应答者分析,意向治疗人群
" i. \8 t6 J& l; r/ N
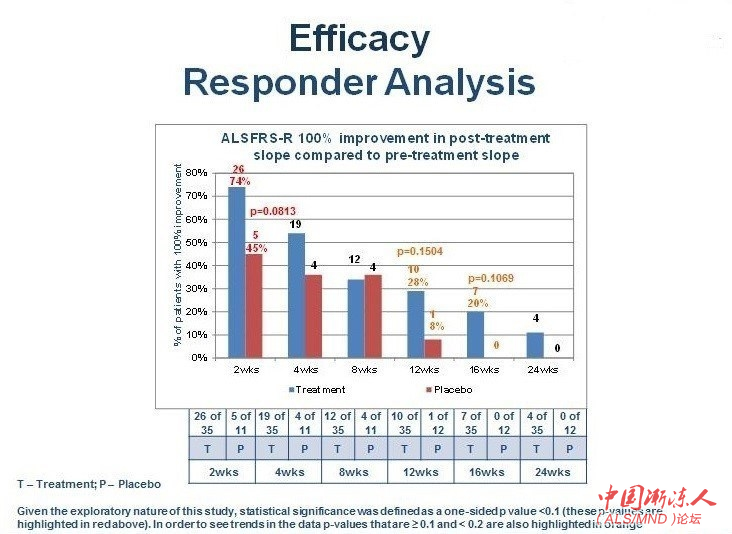
预先规定的应答者分析需要评估治疗后ALSFRS-R斜率与治疗前相比每月的百分比改善和绝对数值(absolute point)改善。首先查看达到25%、50%、75%和100%改善的患者。神经病学家们将斜率的25%改善视作至少具有临床意义,将斜率的50%改善视作非常据有临床意义(Castrillo-Viguera等,《肌萎缩侧索硬化》2010,11:178-180)。
; ~" @9 m: c- U+ E' `
在所有“应答者”定义和除一个时点的所有时点中,与安慰剂组相比,NurOwn治疗组中应答者的比例更高。例如,在第12周(治疗后),NurOwn治疗组中40%患者出现治疗后ALSFRS-R斜率与治疗前相比至少50%的改善,而安慰剂组的比例仅为17%。 ! B1 O1 b3 q# g- }/ L
下面的图表显示了NurOwn治疗患者中可见的益处,应答者使用治疗后ALSFRS-R斜率与治疗前相比100%改善的非常高的阈值进行定义,意味着病情稳定或得到改善的患者才能被定义为应答者。下面的图表展示了NurOwn治疗患者与安慰剂相比的短期和长期益处。
1 L) R4 y3 e1 `. V4 y
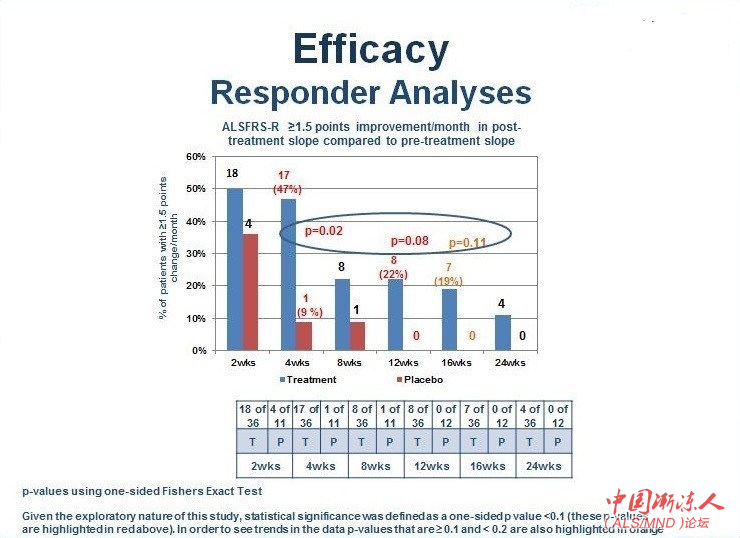
在基于治疗后ALSFRS-R斜率与治疗前相比随时间推移的绝对数值改善/月进行治疗应答评估时,同样获得了NurOwn治疗效果的强有力证据。下面的图表显示了在24周内ALSFRS-R斜率每月改善1.5或更多的患者结果,展示了NurOwn治疗在每个时间点的益处和第4、12和16周统计上显著的(益处)。 ALSFRS-R应答者分析,病情发展较快的子组 ) G" x5 ~% S1 i. e
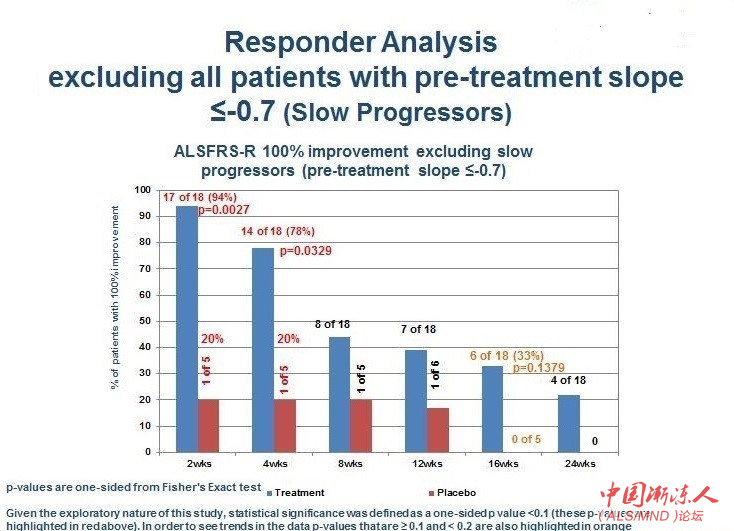
考虑到NurOwn被认为会延缓疾病发展,预先规定了一个排除病情缓慢发展者(治疗前ALSFRS-R斜率为-0.7或更高者)的患者子组。在这些病情缓慢发展的患者中检测到NurOwn治疗益处的可能性较小。病情发展较快的子组占该研究参试者的大约一半,表现出从NurOwn治疗获得显著益处:94%(n=18)在第二周实现斜率的100%改善,而安慰剂组实现这一改善的比例仅为20%(n=5),p=0.0027。第4、8、12、16和24周,治疗组与安慰剂组的应答者比例分别为78%和20%、44%和20%、39%和17%、33%和0%、22%和0%。下面的图表显示了这些结果。
. q5 K/ O Q5 {4 d, t+ m
生物标志物分析
2 i5 S2 e, [2 |2 c
在最初8位患者接受治疗后,按照协议修正案规定,收集了患者的脑脊液样本。共有35份来自移植前和移植后随访的样本可供分析。(研究人员)测定了每份样本中的神经营养因子和炎性因子水平,在应答NurOwn治疗的患者样本中观察到VEGF和HGF水平从移植前到移植后统计上显著增加。在NurOwn治疗的患者中还观察到这一时期炎症标志物(MCP-1和SDF-1)统计上显著减少,而在安慰剂组则没有观察到这一现象。 0 F7 i. G2 e4 d: v* v
安全性 ! @" q3 S) r) m8 ]8 s" t
试验发现,NurOwn是安全而耐受性良好的,大多数不良事件是轻度或中度的。 _: q+ }. v" x3 d. ]
这项研究中没有死亡报告,没有患者因为不良事件而中断治疗。治疗组和安慰剂组的所有患者都至少经历了一次治疗诱发的不良事件。不良事件趋向于轻度到中度。研究人员发现,与安慰剂组相比,治疗组治疗相关不良事件的发生略微更频繁,97.2%比75.0%。频率方面的最大差异是疼痛和背部疼痛的注射部位局部反应以及发热、头痛和关节痛等全身反应。不良事件的模式是一致的,表现为对移植的短暂反应,是较小而自限性的。治疗后严重不良事件(SAEs)方面,治疗组(8/36,22.2%)比安慰剂组(1/12,8.3%)。大部分SAEs与基础的ALS病情发展有关,最常见的是吞咽困难。没有与研究治疗相关的SAEs。MSC-NTF细胞的风险-收益比率仍然是积极的。 , k* p; W1 X. ?9 D; ~& \3 k
* @5 R/ q0 j: `4 b6 m5 w5 Q | 




 发表于 2016-7-19 03:53:43
发表于 2016-7-19 03:53:43

 发表于 2016-7-19 06:50:47
发表于 2016-7-19 06:50:47


 发表于 2016-7-19 07:33:05
发表于 2016-7-19 07:33:05
