1 L/ A8 {7 V: c N; o H2 F
5 }" h7 ~( f$ u) w+ w
' S' y; y' K* b, c% i- \
一项最近发表于《科学报告》(Scientific Reports)的研究发现,移植某些人类骨髓细胞能够通过修复保护脊髓的屏障而改善ALS小鼠的运动功能,并保留运动神经元。 0 l2 l8 X6 P2 B! W8 p1 A
( h: `. u' m. F! \
血脑屏障(BBB)和血脊髓屏障(BSCB)由位于毛细血管壁上的内皮细胞、周皮细胞以及星形胶质细胞的脚板组成。
; X4 u- |6 A: o: ~
越来越多的证据表明,在患者和动物模型中,这些组分的损伤都与ALS有关。如果这些屏障被破坏,免疫细胞和其他潜在有害物质可能从血液循环进入中枢神经系统,加剧ALS的特征——运动神经元变性退化。
6 a1 ?+ B0 f0 o c( W4 y4 R
南佛罗里达大学的研究团队之前在ALS小鼠中表明:包含CD34标志物(hBM34+)的人类骨髓细胞可能成为ALS治疗策略,因为它们能够延迟疾病进展,保护运动神经元生存,减少损伤反应标志物并维护屏障的完整性。移植的细胞分化成内皮细胞,并嵌套在脊髓的毛细血管中。 , Q2 l+ H; G+ l! y) A7 w
在同一小鼠模型(G93A)中进行的后续研究显示,大剂量的移植细胞可以恢复毛细血管的精细结构,稳定它们在脊髓中的密度,同时还能改善髓鞘(保护神经的绝缘层)的完整性。
8 F9 n2 T5 n& O6 T! W4 b4 n/ x, H
尽管这些发现支持使用这些细胞来修复BSCB并改善ALS相关问题,但hBM34+细胞对运动功能最显著的影响是在移植后4周确定的,而且即使是高剂量治疗后依然能检测到脊髓毛细血管的明显损伤。
; y9 E7 _ o! v* {
研究团队因此测试了人类内皮祖细胞(EPCs)——源于骨髓,但比未分化的干细胞更接近内皮细胞——能否在G93A小鼠中提供更好的BSCB修复。
8 l2 n, O6 h5 [( A
" j: W% t3 [/ y( Y0 @! ?- Z
通过静脉输注移植后2到3周,在伸展反射评分、握力和运动协调性的评估方面,接受EPCs的小鼠比对照组体重明显更大、运动功能更好,疾病进展更为缓慢。
% P/ v3 d" E+ e& J- _
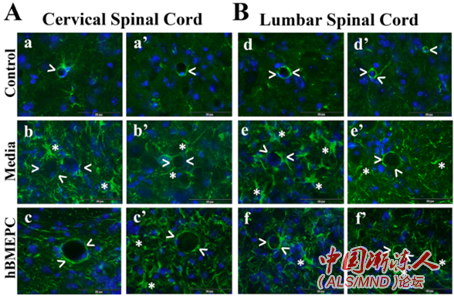
在第4周,这些小鼠还表现出与EPCs广泛附着于颈、腰椎脊髓、大脑运动皮质和脑干中毛细血管相关的BSCB修复,这几个区域以运动神经元退化而闻名。 # ^7 A' o. B- T' @
颈椎和腰椎脊髓的其他改善包括毛细血管和周皮细胞结构的恢复、星形细胞突起的正常化、脊髓内渗漏减少以及脊髓运动神经元生存时间延长。接受移植的小鼠只有一小部分运动神经元出现退化迹象,运动神经元的数量多于对照组。 ( M7 H( o7 B4 Y+ o
在提醒还需要进一步研究的同时,研究团队评论说,“从转化的角度看,在症状发生后的疾病阶段启动细胞治疗,强有力地恢复了BSCB完整性,并显示出作为ALS未来临床疗法的前景。”
3 z- O3 Z% I4 o, }# H
! M; q; z+ j: j" Y( A) u% p
| 




 发表于 2019-4-29 00:53:27
发表于 2019-4-29 00:53:27

 发表于 2019-4-29 01:05:11
发表于 2019-4-29 01:05:11


