PARP抑制剂有望防止脑病蛋白质的毒性积聚
1 |6 v1 _2 V1 f3 {% @. Z8 F" D2 J+ U1 |
费城,2018年8月9日——在一项最新发表于《分子细胞》(Molecular Cell)期刊的研究中,宾夕法尼亚大学艺术与科学学院和佩雷尔曼医学院的研究人员们发现,通过阻止影响神经细胞的特定蛋白质的错位(misplacement),一类被称为PARP抑制剂的癌症药物可用于治疗和预防大脑疾病,包括肌萎缩侧索硬化(ALS)和一些形式的额颞叶变性(FTD)。
8 L. T4 Y, n# ~" U8 U; i7 ^# _0 H, Z
# Y) K/ G5 I: a. H
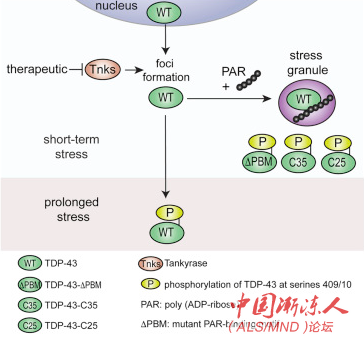
当TDP-43蛋白质错误位于细胞核外时,会在遭受ALS和FTD影响的脑细胞中形成团块。当错误定位的TDP-43结合到另一种分子PAR时,就会积聚在被称为应激颗粒的细胞结构中。虽然最初的积累不会对细胞造成直接的伤害,但在长时间后,TDP-43会改变为在脑病中观察到的结构。现在,生物学教授Nancy Bonini博士和生物化学与生物物理学教授James Shorter博士领导的研究团队发现,阻止PAR生成的PARP抑制剂,减少了处于应激压力下的细胞中有害的TDP-43结构的数量。
- ^2 o' v: `! L3 x$ {0 X
2 U+ x1 Y) g, l6 Y D# J5 I7 z
ALS和FTD-TDP-43这样的疾病对患者及其家庭是毁灭性的,而且目前的治疗选择有限。“追求这一路径让我感到兴奋,因为这些小分子有望攻击TDP-43的疾病过程,” 该研究第一作者、Bonini实验室研究助理Leeanne McGurk博士说,“当我在培养的细胞中进行测试时,我发现它们可以缓解TDP-43的积累。”
) G6 {) X0 R0 O& h4 `9 B/ |
: }& \9 F E, q$ P `
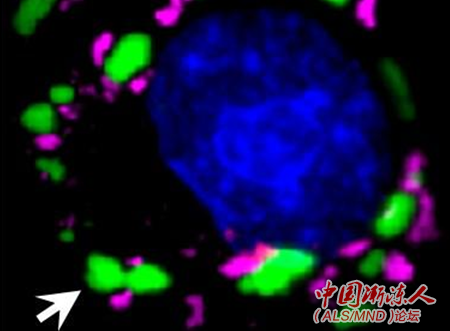
图:在处于应激压力下的细胞中,应激颗粒(洋红色)在细胞核(蓝色)外形成。绿色的TDP-43蛋白(箭头)不能结合到PAR,积累在不同于应激颗粒的大团块中。 * }' c, g, f% Z, m/ D* i0 d8 y
在试管实验中,研究团队发现,TDP-43可以通过与其他TDP-43分子和PAR这样的大分子相互作用而从可溶形式改变成浓缩液体形式。“TDP-43的液体形式是应激颗粒的代表,可能是有益的,” Shorter说道。不过,他指出,如果这些液体形式的TDP-43随时间推移而固化,它们则很难被清除。
R% ~( L+ S8 \3 o
* `2 m+ y( @4 H0 N, G5 \1 ~" g
这项研究的前景在于,一种开发中作为癌症疗法的药物可以用来防止有害的TDP-43团块在细胞中形成。“我们测试的能够对抗TDP-43细胞质积聚的PARP抑制剂可能有朝一日被优化为治疗脑病的宝贵疗法,” 该研究共同作者、Shorter实验室研究专家Edward Gomes说道。
1 \# g( d1 j# Z3 o
虽然这项工作仍在实验室中进行,但研究团队的发现为神经学家寻找对抗神经退行性疾病的新方法提供了接下来的步骤。“由于缺乏治疗选择,我们对这些实验感到兴奋,这些实验有助于阐明可能导向新疗法的分子事件,” Bonini说道。 9 {' ~8 ^9 E* ~9 C
- X2 K- o9 {! i: t& I) {: n4 w# f
6 S: x e* U/ U! D1 u- N# S V | 




 发表于 2018-8-11 01:17:44
发表于 2018-8-11 01:17:44



 发表于 2018-8-11 01:38:45
发表于 2018-8-11 01:38:45

 发表于 2018-8-11 06:33:11
发表于 2018-8-11 06:33:11

 兄弟辛苦了
兄弟辛苦了